Op dit moment bevindt de gezondheidszorg zich voor biosimilars op een belangrijk keerpunt. Vergelijkbaarheid, inclusief de uitwisselbaarheid tussen biosimilars en referentiegeneesmiddelen zoals de European Medicines Agency (EMA) aangeeft, is steeds meer geaccepteerd. En huisartsen en specialisten die ervaring hebben met biosimilars erkennen de voordelen ervan. Marktonderzoeksbureau IQVIA heeft uitgerekend dat tussen 2006 en 2021 in Europa ongeveer 4,2 miljard behandeldagen met biosimilars hebben plaatsgevonden.
Dat biedt kansen voor het gezondheidszorgsysteem om optimaal van de besparingsmogelijkheden te profiteren zodra nieuwe biosimilars zich aandienen. Besparingen die we kunnen gebruiken om nieuwe behandelingen te betalen en meer patiënten met een biologisch geneesmiddel te behandelen. IQVIA schat zelfs in dat belangrijke biosimilars en generieke geneesmiddelen die naar verwachting de komende vijf jaar voor Multiple Sclerose (MS) beschikbaar komen in die 5 jaar € 4,5 tot € 5,5 miljard aan besparingen in Frankrijk, Duitsland, Italië, Spanje en het Verenigd Koninkrijk (ook wel de EU-5 genoemd) kunnen opleveren. Maar hiervoor is wel een voorwaarde: tijdig de opname van biosimilars in de markt op een toekomstbestendige manier organiseren.
Terwijl generieke geneesmiddelen meestal goed en vlot worden opgenomen in de markt, is dat voor biosimilars anders. We zien daarin grote verschillen tussen landen en daar kunnen we van leren. Er is voor de biosimilarmarkt geen ‘one size fits all’-aanpak. Elk indicatiegebied, ieder type patiënt en ieder type medisch specialist vraagt een aanpak op maat. Dat laat figuur 1 mooi zien.
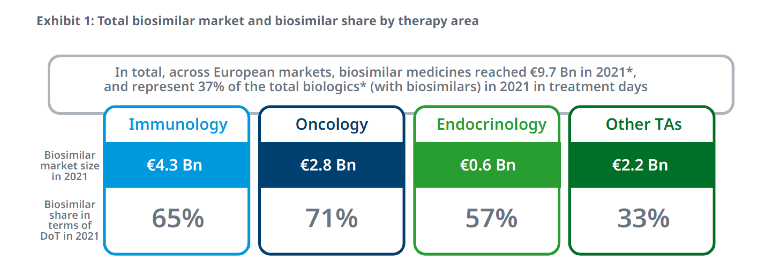
De biosimilar verkopen ‘af fabriek’ waren in 2021 bijna € 10 miljard. Het aandeel biosimilars van de totale hoeveelheid biologische geneesmiddelen (uitgedrukt in patiënt-behandeldagen) verschilt echter per indicatiegebied (van 30% tot 71%).
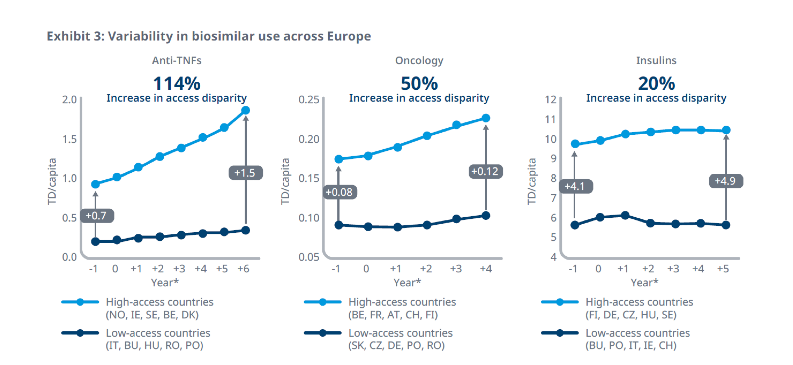
In figuur 3 zien we de landen in Europa met een hoge biosimilaropname in lichtblauw en de landen met een lage biosimilaropname in donkerblauw. Bij de insulines zien we weinig groei (redelijk verzadigde markt) in biosimilargebruik. Bij de oncologische middelen zien we dat de groei in het aantal patiënten met een biosimilar in landen met hoge biosimilaropname ongeveer 50% groter is dan in de landen met lage biosimilaropname. Bij de TNF-alfaremmers zoals infliximab, etanercept en adalimumab is het verschil in groei dramatisch groot. Het zijn vooral de Oost-Europese landen waar sprake lijkt te zijn van sterke onderbehandeling met biosimilars.
Verder is het belangrijk om de verschillen tussen generieke geneesmiddelen en biosimilars te herkennen, omdat biosimilars complexer zijn om te ontwikkelen en te produceren. En omdat de voorkeuren van artsen of patiënten bij biosimilars sterker kunnen zijn. IQVIA stelt dat voor een toekomstbestendige biosimilarmarkt het cruciaal is dat:
- alle belanghebbenden, dus betalers, ziekenhuizen, fabrikanten, artsen en patiënten daar op een zichtbare wijze voordeel van hebben
- er respect is voor de voorschrijfverantwoordelijkheid van artsen en
- er gezonde concurrentie is
Winstdeling blijkt bijzonder zinvol beleid te zijn bij artsen, omdat het directe voordelen oplevert voor zowel artsen, zorginstellingen als betalers. Daarnaast is ook scholing van artsen en patiënten over biosimilars cruciaal, zonder aan de voorschrijfverantwoordelijkheid van artsen te komen. Voor dit laatste punt zet Biosimilars Nederland zich al jaren in.
Voor autonomie van arts en patiënt, kostenbesparingen en een toekomstbestendige biosimilarmarkt is een zorgvuldig beleid nodig. De ervaring laat namelijk zien dat het lang niet overal lukt om te profiteren van de voordelen door concurrentie met biosimilars. Bijvoorbeeld als voor of tijdens de introductie van een intraveneuze biosimilar het referentiegeneesmiddel met een subcutane versie komt, zoals bij trastuzumab het geval was. De biosimilar moet dan concurreren met deze nog door een patent beschermde subcutane versie. En als de patiënt voor intraveneuze toediening naar het ziekenhuis moet, kan de voorkeur uitgaan naar het subcutane referentiegeneesmiddel dat de patiënt in een aantal gevallen thuis zelf kan toedienen.
Dus zelfs als het referentiegeneesmiddel en de biosimilar een vergelijkbare veiligheid en werkzaamheid hebben en de biosimilar kostenbesparingen oplevert, kan de keuze voor de biosimilar een uitdaging zijn. Met de komst van biosimilars in de neurologie, zoals natalizumab voor MS moeten we nu de scholing van – en communicatie naar zorgprofessionals en patiënten van meet af aan goed aanpakken. Laten we daarom als maatschappij, in gezamenlijkheid als overheid, zorgverzekeraars, zorgprofessionals en patiënten gebruikmaken van de ervaringen die bij de verschillende specialistengroepen al zijn opgedaan en zorgen voor een toekomstbestendige biosimilarsmarkt. Anders betekent dat een gemiste kans voor de behandeling van patiënten!
Wat betekent dit rapport voor de neurologen en MS-patiënten in Nederland?
De scholing over biosimilars van deze nieuwe groep specialisten en patiënten moet op gang komen, zodat zij met de kennis en ervaring bij andere specialistengroepen zelf ook kunnen ervaren dat biosimilars een gelijkwaardig alternatief zijn voor het referentiemiddel. Vooralsnog komt er alleen een intraveneuze vorm van de biosimilar natalizumab. Daarom adviseren wij de neurologen om terughoudend te zijn in het nu omzetten van patiënten met de intraveneuze vorm van het originele referentiegeneesmiddel Tysabri® (natalizumab) naar een subcutane vorm. En zich alvast te beraden op hoe zij patiënten die reeds worden behandeld met de subcutane vorm van Tysabri® kunnen omzetten naar de intraveneuze vorm, dit alles in goed overleg met deze patiënten. Dat dit goed mogelijk is hebben we gezien aan de omzetting van trastuzumab en van rituximab van subcutaan naar intraveneus, dat in Nederland op grote schaal goed is gegaan.
Wilt u meer weten? Lees dan het IQVIA-Rapport Unlocking Biosimilar Potential.
Referentie
- IQVIA Institute for Human Data Science. Unlocking Biosimilar Potential. 2023 Apr. Zie https://www.iqvia.com/insights/the-iqvia-institute/reports/unlocking-biosimilar-potential.

Volg ons via: