Farmaceutische bedrijven gebruiken allerlei strategieën om hun investering in een nieuw geneesmiddel te beschermen met patenten en andere Special Protection Certificates (SPC’s). In de loop van de tijd worden bij een geneesmiddel nieuwe indicaties uitgezocht en daarna gepatenteerd. Daarmee wordt de patentbescherming van zo’n middel opgerekt. Biosimilarfabrikanten kunnen die indicaties niet voeren bij hun middel dat in de regel is gebaseerd op de eerst aflopende patenten. Een biosimilarfabrikant heeft dan twee opties: wachten tot alle patenten zijn afgelopen of de biosimilar registreren met gekortwiekte indicaties. Het gevolg is dat biosimilars regelmatig met een gekortwiekte lijst van indicaties worden geregistreerd (skinny label genaamd) en niet bij alle indicaties kunnen worden voorgeschreven. Dat beperkt natuurlijk het besparingspotentieel van zo’n biosimilar. Maar iets is beter dan niets….
Egilman en collega’s hebben uitgezocht hoe vaak zo’n biosimilar met gekortwiekte indicaties door de Food and Drug Administration (FDA) is goedgekeurd tussen 2025 en 2021. En wat voor besparing zo’n biosimilar opleverde voor het Amerikaanse Medicare-zorgsysteem. Hun bevindingen staan in het JAMA Internal Medicine van Januari 2023. Een bladzijde verder staat er een redactioneel commentaar van Ward en Steinbrook.
Bevindingen
Tussen 2015 en 2021 keurde de FDA 33 biosimilars goed, verwijzend naar 11 referentieproducten. Tweederde van de goedgekeurde biosimilars hadden gekortwiekte indicaties, verwijzend naar 8 referentieproducten. Skinny labels komen bij initiële registraties dus vaak voor. Figuur 1 geeft dat grafisch weer.
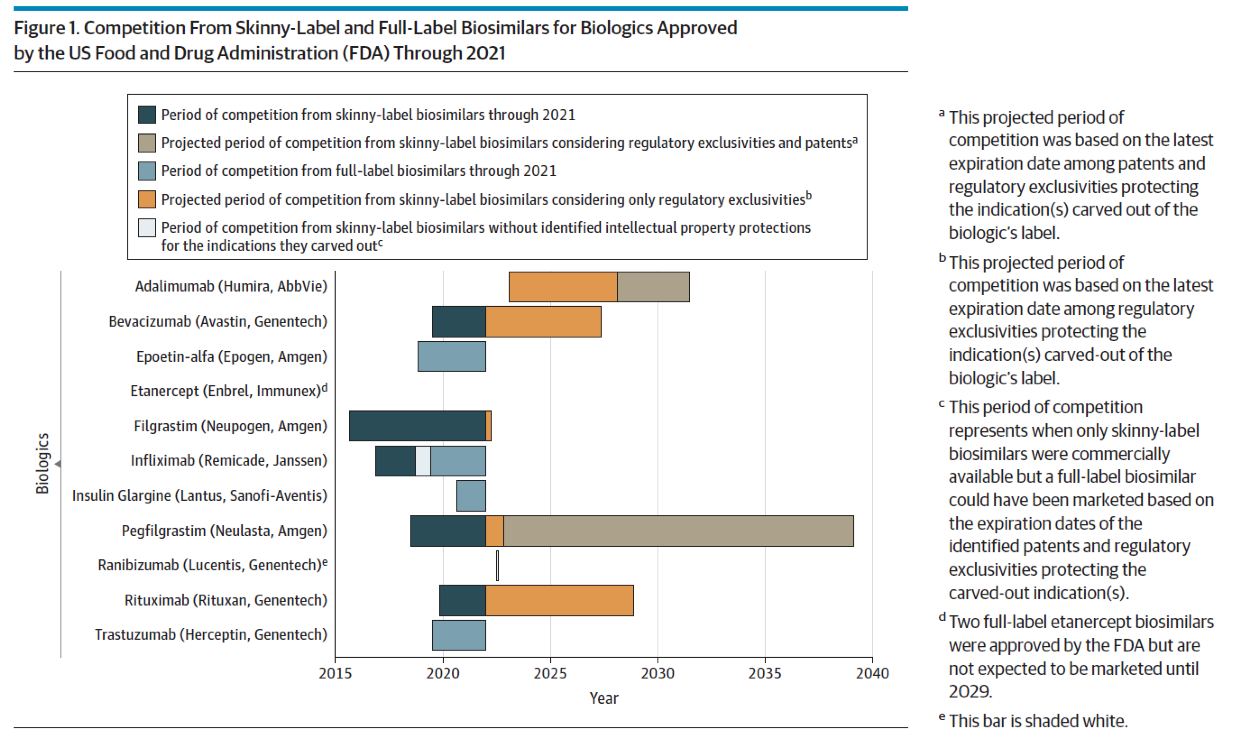
De auteurs berekenden dat deze gekortwiekte biosimilars voor vijf verschillende referentieproducten het Medicare-zorgsysteem van 2015 tot en met 2020 totaal zo’n 1,5 miljard dollar hebben bespaard op een totaal aan uitgaven van 30 miljard dollar (5%). Zie figuur 2 uit het artikel.
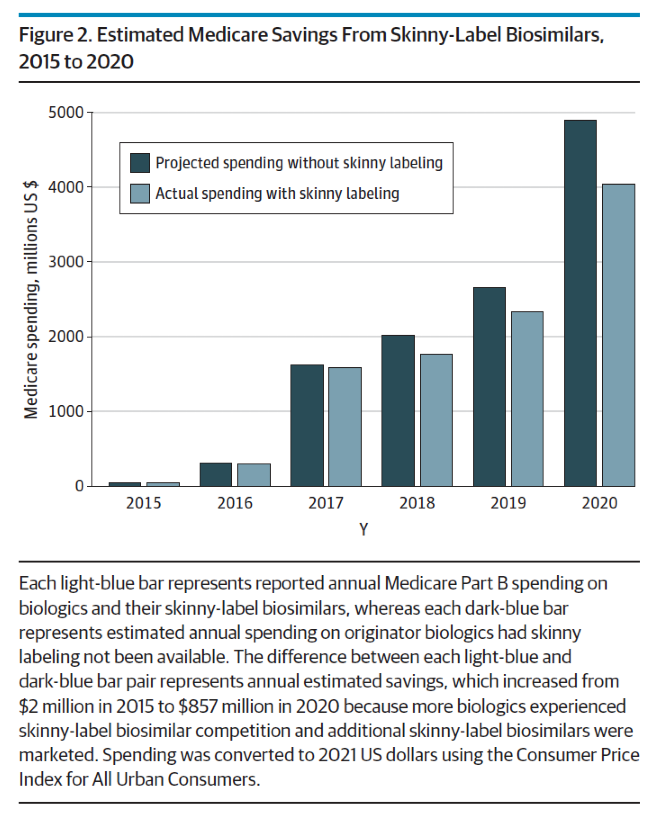
Zij stellen daarom dat het vroeg toelaten van gekortwiekte biosimilars wel degelijk zin heeft. Beter dan te wachten tot alle indicaties vrijvallen van patent. Dit jaar vervalt het hoofdpatent voor Humira® en komen de biosimilars in de Verenigde Staten gekortwiekt op de markt. Niettemin verwachten de auteurs sterk toegenomen besparingen.
In een commentaar van de redactie gaan Ward en Steinbrook hier verder op in. Zij stellen dat biosimilars eenzelfde patroon volgen als eerder gebeurde met generieke (chemische) geneesmiddelen. En ze stellen dat vroege registratie van biosimilars (en generieke middelen) zelfs met een ingeperkt aantal indicaties heel nuttig kan zijn voor de betaalbaarheid en toegankelijkheid van geneesmiddelen voor patiënten. Zij roepen daarom het Amerikaanse congres op geen gehoor te geven aan de lobby die de innovatieve farmaceutische industrie is gestart om toelating van skinny label biosimilars tegen te gaan. En de toelating vooral doorgang te laten vinden. Daarvoor zijn de voordelen voor patiënten te groot. Skinny labels zijn niet fraai, maar voor patiënten die deze middelen nodig hebben wel een uitkomst.
Referenties
- Egilman AC, Van de Wiele VL, Rome BN, et al. Frequency of Approval and Marketing of Biosimilars With a Skinny Label and Associated Medicare Savings. JAMA Intern Med. 2023;183(1):82-84. doi:10.1001/jamainternmed.2022.5419
- Ward E, Steinbrook R. Savings Associated With ‘Skinny Label’ Biosimilars. JAMA Intern Med. 2023;183(1):84. doi:10.1001/jamainternmed.2022.5418

Volg ons via: